Mycobacterium tuberculosis
Mycobacterium
tuberculosis (Koch 1882)
Familie: Mycobacteriaceae
D: Tuberkelbazillus
E: tubercle bacilli
F: bacille de la tuberculose
1.
Parasit, Übertragung und Vorkommen
2. Diagnostik
3. Wirt-Parasitinteraktion
4. Infektion und Krankheit
5. Epidemiologie
6. Kontrollstrategien
7. Kernsätze
8. Ressourcen
1.
Parasit, Übertragung und Vorkommen
top
1.1. Parasit
M. tuberculosis gehört mit anderen Mycobakterien (u.a. M. bovis,
M. africanum) zum M. tuberculosis-Komplex. Verwandte Mycobakterien sind
M. leprae (Erreger der Lepra) und M. ulcerans (Erreger des Buruli-Ulkus,
einer Hautinfektion mit schwerer Schädigung).
Die Tuberkelbazillen sind aerobe, unbewegliche Stäbchen (ca. 0.2-0.5
µm auf 2-5 µm), die sich intrazellulär vermehren. Sie
werden als säurefest bezeichnet, weil sie sich im Gegensatz zu den
meisten Bakterien in verdünnten Säuren nicht entfärben.
Dies wird für den mikroskopischen Nachweis ausgenutzt. Die besonderen
Eigenschaften der Mycobakterien wie Komplementresistenz, Zytoadhärenz
u.a. sind durch Struktur und Chemie der komplexen Zellwand bedingt. Diese
enthält Glykolipide, Wachse und Polysaccharide.
Das Genom mit 4.4 Millionen Basenpaaren wurde 1998 vollständig sequenziert.
Dies vereinfacht die Suche nach Virulenz-Genen, Impfstoff-Antigenen und
neuen Medikamenten.
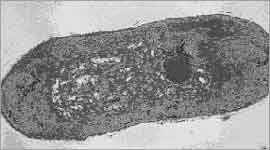
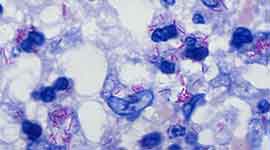
Mycobacterium tuberculosis;
Säurefeste Tuberkelbazillen in einem Lungengranulom (rote Stäbchen);
1.2.
Übertragung
Tuberkelbazillen werden meist aerogen ("Tröpfcheninfektion"),
viel seltener oral (z.B. mit Milch von infizierten Kühen!) und Hautverletzungen
übertragen. Die Tuberkelbazillen sind zum Glück nicht hoch ansteckend.
1.3. Vorkommen
Die Tuberkulose kommt weltweit vor. Es wird angenommen, dass jeder 3.
Mensch (=d.h. fast 2 Milliarden!) von Tuberkelbazillen (latent) infiziert
ist. Die WHO schätzt, dass jedes Jahr 3 Millionen Menschen an Folgen
einer Tuberkulose sterben. Die jährlichen Inzidenzraten sind –
ausgenommen in der westlichen Welt – in den letzten Jahren am Steigen.
2.
Diagnostik
top
Der direkte Erregernachweis in Kultur (Löwenstein-Jensen Nährmedium)
ist nach wie vor der Goldstandard und beweisend, benötigt jedoch
mehrere (meist 3-4, bis 8) Wochen.
Statt der Ziehl-Neelsen Färbung mit Karbolfuchsin (die nicht absolut
spezifisch für M. tuberculosis ist) und anschliessender Mikroskopie
lässt sich der Erreger heute innerhalb eines Tages mittels PCR (Polymerasen-Kettenreaktion)
nachweisen.
Mit dem Tuberkulin-Hauttest ("Mantoux-Reaktion") wird eine spezifische
T-Zell-Aktivierung (sog. verzögerte Überempfindlichkeitsreaktion)
mittels PPD (purified protein derivative of tuberculin) nachgewiesen.
Diese zeigt sich durch eine Verhärtung, Schwellung und Rötung
der Haut, die frühestens nach 24 Stunden auftritt. Der Test wird
am 2. oder 3. Tag abgelesen.
Pathologische Prozesse in der Lunge können mittels Röntgenaufnahmen
nachgewiesen werden.
Eine Antibiotika-Resistenzbestimmung ist wichtig, da die Spontanmutationsrate
der Mycobakterien hoch ist.

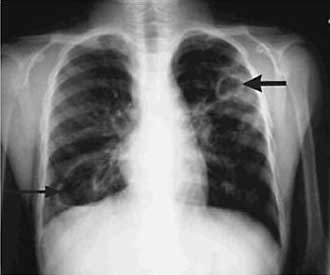
Untersuchung von Sputumproben unter dem Lichtmikroskop, Navrongo, Ghana; WHO/TDR/CRUMP
Tuberkulose im Thoraxröntgenbild;
3.
Wirt-Parasitinteraktionen
top
Spezifische Aspekte im Überblick:
3.1 Phagozytose durch alveolare Makrophagen
3.2 Überlebensstrategie in Wirtszellen (Makrophagen)
3.3 Die latente Tuberkulose (TB) - immer noch ein Rätsel!
3.4 Krankmachende Immunantworten (Granulombildung)
3.5 Faktoren, welche die Empfänglichkeit des Wirtes beeinflussen
3.1
Phagozytose durch alveolare Makrophagen
In der Regel erreichen Tuberkelbazillen über die Atemluft
die Lunge und werden von alveolaren Makrophagen aufgenommen. Um eine Phagozytose
einzuleiten, muss eine enge Bindung (Zytoadhärenz) zwischen Pathogen
und Wirtszelle realisiert werden. Verschiedene Rezeptoren auf der Makrophagen-Membran
(am bedeutendsten der Komplementrezeptor CR3, auch CR1 und CR4, sowie
der Mannose-Rezeptor) interagieren direkt mit Zuckerresten auf verschiedenen
Oberflächenmolekülen der Tuberkelbazillen sowie mit Wirtsmolekülen
(etwa die Komplementkomponente C3b), welche mit dem Parasiten eine Bindung
eingegangen sind. Es sind also multiple Rezeptor-Ligandsysteme bei der
Zytoadhärenz von Mycobakterien an Makrophagen involviert. Es scheint,
dass Mycobakterien es darauf anlegen, von Makrophagen aufgenommen zu werden.
Weshalb? Vorteile der intrazellulären Lokalisation könnten im
einfacheren Transport durch Lungenepithelien und damit in einer besseren
Verbreitung liegen.
3.2
Überlebensstrategie in Wirtszellen (Makrophagen)
In der Regel werden aufgenommene Parasiten in Phagolysosomen des Makrophagen
abgebaut. Dies geschieht auch mit abgetöteten Tuberkelbazillen. Lebende
Tuberkelbazillen vermögen aber, die Fusion von Phago- und Lysosom
zu verhindern. Dabei spielen gewisse Proteine ("TACO-Proteine")
der Wirtszelle eine wichtige Rolle, die sich eng mit der Phagosomenmembran
verbinden. Im weiteren Verlauf wird die Makrophagen-Physiologie durch
die intrazellulären Parasiten verändert: Es werden weniger MHC-Klasse
II-Moleküle exprimiert, und die Produktion von inhibitorischen Zytokinen
(wie etwa IL-10 und TGF-beta) wird erhöht.
3.3 Die latente Tuberkulose (TB) - immer noch ein Rätsel!
Infektiöse Tuberkelbazillen können vom Immunsystem über
Jahrzehnte in Schach gehalten werden. Tierexperimentelle Untersuchungen
weisen darauf hin, dass das Zusammenspiel der verschiedenen T-Zell Populationen
essentiell für die Abwehr der TB ist. Untersuchungen am Tier sind
nicht möglich, da es kein subklinisches (d.h. latente Infektion ohne
Krankheit) Tiermodell gibt. Hier spielen Th1 Immunantworten von CD4-positiven
T Zellen und die durch IFN-gamma aktivierten Makrophagen eine wichtige
Rolle. Aber auch CD8-positive T-Zellen können durch die Ausschüttung
von Granulysin und Perforin intrazelluläre Mycobakterien abtöten.
Die Bedeutung von T-Zellen und CD1-restringierten CD8-positiven T-Zellen,
welche Lipide erkennen und IFN-gamma ausschütten, ist noch nicht
abschliessend geklärt. Antikörper haben keine Bedeutung für
die Wirtsabwehr.
Bei 2-23% aller Infizierten (während ihrer gesamten Lebensdauer)
kommt es zu einer Reaktivierung der Infektion und zur Krankheit. Es scheint
dass Parasit und Wirt sich über lange Zeit in einem (labilen) Gleichgewichtszustand
befinden.
Ob dabei Mycobakterien in alten Primärläsionen "erwachen"
oder Herde ausserhalb der Lunge eine Rolle spielen, ist noch offen. Auch
ist es unklar, ob sich bis zum Zeitpunkt der Reaktivierung die Mycobakterien
in einem Zustand des nicht-proliferativen Wachstums oder in einer metabolischen
Inaktivität (Sporen-ähnlicher Zustand) befinden. Medikamente
vermögen nicht, den Erreger in der Latenzphase zu eliminieren, vermindern
aber das Risiko einer Reaktivierung.
Die Wahrscheinlichkeit einer Reaktivierung einer latenten TB wird durch
eine HIV-Infektion, durch immunsuppressive Therapie, durch Krebs, Diabetes,
Mangelernährung sowie hohes Alter erhöht. Bei einer HIV-Infektion
steigt das Risiko einer reaktivierten TB auf 5 - 10% pro Jahr.
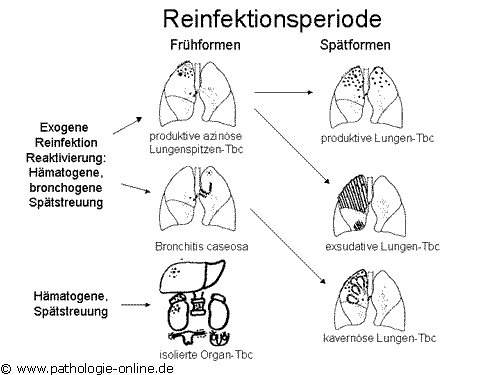
3.4
Krankmachende Immunantworten (Granulombildung)
Es scheint, dass die Immunabwehr gegen Tuberkelbazillen weitgehend für
die Pathogenese verantwortlich gemacht werden kann. Die Proliferation
der Tuberkelbazillen lockt durch chronische Entzündungsprozesse Phagozyten
(Polymorphkernige Granulozyten und Makrophagen) sowie T Zellen an. Makrophagen
verschmelzen zu Riesenzellen. Wenn die Tuberkelbazillen nicht abgetötet
werden können, bildet sich um den Infektionsherd eine Zellschicht
mit einer dicken Fibrosewand. Dieser Prozess wird als Granulombildung
bezeichnet. Die Läsion mit den eingeschlossenen Tuberkelbazillen
wird als Tuberkel bezeichnet. Zu Läsionen des Lungengewebes kommt
es, weil Makrophagen bei ihrem Versuch, Tuberkelbazillen zu zerstören,
Lysozyme und Tumornekrosefaktor (TNF)-alpha abgeben, welche Wirtszellen
abtöten. Der bei einer TB verursachte Gewichtsverlust wird ebenfalls
TNF-alpha zugeschrieben. Aus diesem Grund hiess dieses Zytokin früher
Kachexin. Werden Granulome durch diese Prozesse aufgelöst, so können
sich Tuberkelbazillen ausbreiten. Tuberkel können aber auch verkalken.
Damit werden sie auf dem Röntgenbild sichtbar.
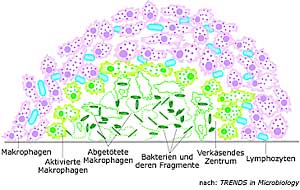
Granulomaufbau
Im Zentrum ist das Granulom nekrotisch und es werden extrazelluläre
Mycobakterien gefunden. Wenn Kavernen entstehen, können diese die
Luftwege erreichen. Um das nekrotische Zentrum befinden sich Makrophagen
mit intrazellulären Bakterien. In der Randzone findet man Lymphozyten.

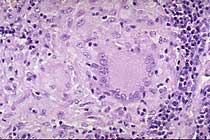
Granulom in einem Lymphknoten; www.pathologie-online.de
Schematische Darstellung eines Granuloms; TRENDS in Microbiology
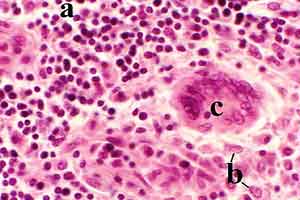
Granulom in der Lunge;
a: Lymphozyten, b: Makrophagen, c: Riesenzellen; www.pathologie-online.de
3.5
Faktoren, welche die Empfänglichkeit des Wirtes beeinflussen
Unsere Kenntnisse, weshalb es bei manchen Infizierten zu schwerer Erkrankung
kommt, sind noch gering. Es wird angenommen, dass Variabilitäten
in gewissen Genen, welche die Immunabwehr kontrollieren, dafür verantwortlich
gemacht werden können.
Literatur: Jean-Laurent Casanova and Laurent Abel: GENETIC DISSECTION
OF IMMUNITY TO MYCOBACTERIA: The Human Model Annu. Rev. Immunol., Vol.
20: 581-620.
4.
Infektion und Krankheit
top
Was versteht man unter einer TB Infektion? Die Konversion von einem negativen
zu einem positiven Hauttest ist Zeichen einer Infektion und zeigt an,
dass Tuberkelbazillen (die sich nicht leicht nachweisen lassen) überlebt
haben. Amerikanische Ärzte lehnen - nicht nur wegen der fraglichen
Schutzwirkung - die BCG-Impfung ab, weil diese ebenfalls eine Konversion
des Hauttests bewirkt.
Nur 3 bis 5 % der Menschen, die ohne BCG-Impfung Hauttest positiv werden,
werden krank. Die meist langsam fortschreitende Krankheit äussert
sich mit Fieber, Husten (oft mit blutigem Sputum), Gewichts- und Energieverlust.
Die Lunge wird irreversibel zerstört. Die Tuberkelbazillen können
sich von der Lunge in andere Organe (u.a. Leber, Milz, Gehirn) verbreiten.
Man spricht dann von einer generalisierten oder einer Miliartuberkulose.

Miliartuberkulose;
www.pathologie-online.de
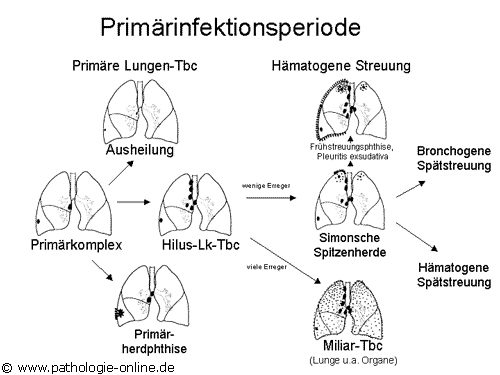
Primärtuberkulose
Die Primärtuberkulose entwickelt sich aus dem Primärkomplex,
welcher aus einem lokalen Entzündungsherd (meist in der Lunge) besteht.
Im häufigsten Fall läuft eine Primärtuberkulose symptomlos
ab. In ca. 5% der Fälle können Fieber und grippeähnliche
Symptome auftreten. Die zelluläre Immunität hält den Parasiten
im Schach. Bei geschwächter Immunität, z.B. durch eine HIV-Infektion,
eine immunsuppressive Therapie oder im hohen Alter, kommt es zu einer
Reaktivierung der latenten Infektion.
Postprimäre Tuberkulose
Diese entsteht durch Streuung von Mycobacterien aus einem frischen Primärkomplex,
aus alten Herdbildungen oder durch eine Superinfektion. Dabei handelt
es sich meist (in 85% der Fälle) um einen Lungenaffekt. Die Granulome
sind grösser als bei einer Primär-TB und es können durch
verkäsende Nekrosen Kavernen gebildet werden. Damit entsteht eine
"offene" Tuberkulose, die das gesamte Bronchialsystem befällt.
Der infizierte Wirt ist damit zur Ansteckungsquelle geworden. Auch andere
Organe können über den Blutweg besiedelt werden ("Miliartuberkulose").

Tuberkulöse Kaverne in der Lunge; www.pathologie-online.de
Wegen der Besonderheiten des Zellwandaufbaus können nur spezielle Antibiotika eingesetzt werden. Eine längerfristige Kombinationstherapie - um eine Resistenzentwicklung zu minimieren - ist erforderlich. Von der Weltgesundheitsbehörde (WHO) wird empfohlen, nach einer zweimonatigen Kur mit 4 Medikamenten eine viermonatige Behandlung mit Isoniazid und Rifampicin durchzuführen. Die Heilungsrate beträgt etwa 85%.
Rechts: Ein Kind wird mit Isoniazid-Tabletten behandelt, Buenos Aires, Argentinien; WHO/TDR/Crump
5.
Epidemiologie
top
Die TB kommt weltweit endemisch vor. Mit geschätzten 3 Millionen
Todesfällen pro Jahr gehört sie zu den "big killer diseases".
Weiter schätzt man, dass ca. jeder 3. Mensch latent infiziert ist,
wobei diese Menschen ohne Reaktivierung zum Glück kein Infektionsreservoir
darstellen. Die AIDS-Pandemie hat zur Folge, dass die Inzidenz der TB
im Steigen ist. Ein Drittel der HIV-Todesfälle in Entwicklungsländern
ist durch eine TB bedingt.
Weil unbehandelt eine Tuberkulose in 50% der Fälle tödlich verläuft, haben Tuberkelbazillen als Selektionskriterium während der menschlichen Evolution eine Bedeutung.
Im
Internet finden Sie einen Powerpoint-Kurs mit dem Titel: "Epidemiology
of Tuberculosis"
http://www.pitt.edu/~super1/lecture/lec0711/index.htm
6.
Kontrollstrategien
top
- Aktive Fallsuche von TB Patienten.
- Kontrollierte Behandlung (Direct Observation Therapy Short Course; DOTS) bei aktiven TB-Fällen über 6 Monate.
- Expositionsprophylaxe für Angehörige eines TB Falles.
- Massnahmen zur sozio-ökonomischen Verbesserung der Lebensbedingungen (Ernährung, Wohnen u.a.).
- Entwicklung einer neuen Impfung.
Die
BCG Impfung wird nicht mehr empfohlen!
Durch jahrelange Kultivation wurde ein ursprünglich für Kälber
und Meerschweinchen virulentes M. bovis Isolat attenuiert und als Bacille
Calmette Guérin (BCG) Impfstoff erstmals in den 20iger Jahren angewendet.
Meta-Analysen von Impfversuchen zeigen unterschiedliche Resultate und
es ist heute sehr umstritten, ob eine BCG-Impfung wirklich schützt.
Es ist auch zu schweren Impfzwischenfällen gekommen (wie etwa in
Lübeck, 1926), wo Kinder mit TB infiziert worden sind! Neue genetische
Analysen haben gezeigt, dass die heute verwendeten BCG-Stämme nicht
homogen sind. Das könnte die unterschiedlichen Resultate erklären.
Da das Infektionsrisiko für Kinder in Mitteleuropa unter 0,015% liegt
und eine Impfung eine Infektion wahrscheinlich nicht verhindern kann,
sondern nur eine Verminderung des Risikos einer Miliartuberkulose und
einer tuberkulösen Meningitis bewirkt, ist eine generelle Impfung
aller Säuglinge epidemiologisch und ethisch nicht vertretbar. Es
besteht keine Indikation zur Impfung Erwachsener, da eine Schutzwirkung
bislang nicht nachgewiesen werden konnte. Bei exponierten Erwachsenen
ist deshalb generell die Chemoprophylaxe einer BCG-Impfung vorzuziehen.
Erwünschte Eigenschaften einer neuen Vakzine wären:
- Eliminierung der Tuberkelbazillen bei der Erstinvasion
- Kontrolle von Reaktivierung oder Reinfektion
- Wirkung
als Immuntherapie bei Vielfachresistenz
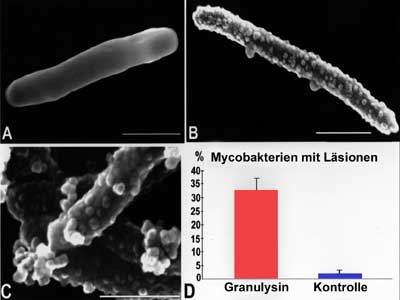
Wirkung von Granulysin auf Mycobakterien
Blindtext
© Steffen Stenger
7.
Kernsätze
top
- Mycobacterium tuberculosis ist ein aerobes, säurefestes und stabförmiges Bakterium, das sich intrazellulär vermehrt.
- Eine Infektion mit Tuberkelbazillen führt in lediglich 3-5% der Fälle zu einer Krankheit, deren Verlauf chronisch ist.
- Die meisten Infektionen bleiben klinisch latent (d.h. ohne Symptome).
- In klinisch latenten Infektionen bleiben die Tuberkelbazillen am Leben und können bei einer Schwächung der Immunabwehr, wie sie bei einer HIV-Infektion auftritt, eine reaktivierte Tuberkulose auslösen. AIDS-Patienten haben ein 10%iges Risiko pro Jahr, an Tuberkulose zu erkranken.
- Tuberkulose ist ein weltweites Problem. Man geht davon aus, dass etwa ein Drittel der Weltbevölkerung mit Tuberkelbazillen infiziert ist.
- Tuberkelbazillen lassen sich von Monozyten und Makrophagen aufnehmen, entgehen aber der Zerstörung durch clevere Evasionsstrategien wie etwa der Verhinderung einer Fusion von Phago- und Lysosom.
- Die Pathogenese der Tuberkulose hängt weitgehend mit krankmachenden Immunantworten zusammen.
- Zu den Kontrollstrategien gegen TB zählen die aktive Fallsuche von TB-Patienten, die kontrollierte Behandlung bei aktiven TB-Fällen über 6 Monate, eine Expositionsprophylaxe für Angehörige sowie Massnahmen zur sozio-ökonomischen Verbesserung der Lebensbedingungen.
- Zur Zeit gibt es keine wirksame Vakzine, eine BCG-Impfung wird nicht
mehr empfohlen.
8.
Ressourcen
top
Lehrbuch
“Medizinische Mikrobiologie” (10. Auflage), Kayser et al.,
Thieme-Verlag: Mycobakterien, Tuberkulose (Seiten 273 bis 282)
CD-ROM "Tuberculosis" (Topics in International Health) vom Wellcome
Trust (in der Bibliothek erhältlich)
Originalarbeiten:
Minireview01.pdf
Tuberculosis: Latency and Reactivation
Joanne L. Flynn & John Chan
Infection and Immunity 69 (7), 4195-4201 (2001)
URLs:
http://www.lungusa.org/diseases/lungtb.html